Этиловый спирт – формула и применение. Какая химическая формула этилового спирта
Перейти к: навигация, поиск
| Систематическое наименование |
Этанол |
| Традиционные названия | Этиловый спирт |
| Хим. формула | С2H5OH |
| Рац. формула | СH3СH2OH |
| Физические свойства | |
|---|---|
| Состояние | жидкость |
| Молярная масса | 46,069 г/моль |
| Плотность | 0,7893 г/см³ |
| Поверхностное натяжение | 22,39×10−3 Н/м при 20 °C Н/м |
| Термические свойства | |
| Т. плав. | -114,3 °C |
| Т. кип. | +78,4 °C |
| Т. всп. | 13 °C |
| Т. свспл. | +363 °C |
| Пр. взрв. | 3,28 - 18,95 % |
| Тройная точка | -114,3 °C, ? Па |
| Кр. точка | +241 °C, 63 бар |
| Мол. теплоёмк. | 112,4 Дж/(моль·К) |
| Энтальпия образования | −234,8 кДж/моль |
| Химические свойства | |
| pKa | 15,9 |
| Растворимость в воде | неограничена |
| Оптические свойства | |
| Показатель преломления | 1,3611 |
| Структура | |
| Дипольный момент | (газ) 1,69 Д |
| Классификация | |
| Рег. номер CAS | 64-17-5 |
| PubChem | 702 |
| Рег. номер EINECS | 200-578-6 |
| SMILES | CCO |
| Кодекс Алиментариус | E1510 |
| RTECS | KQ6300000 |
| ChemSpider | 682 |
| Безопасность | |
| ЛД50 | 10 300 мг/кг |
| Токсичность | метаболит, малотоксичен |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Этано́л (эти́ловый спирт, метилкарбино́л, ви́нный спирт или алкого́ль, часто в просторечии просто «спирт») - одноатомный спирт с формулой C2H5OH (эмпирическая формула C2H6O), другой вариант: CH3-CH2-OH, второй представитель гомологического ряда одноатомных спиртов, при стандартных условиях летучая, горючая, бесцветная прозрачная жидкость.
Действующий компонент алкогольных напитков, являющийся депрессантом - психоактивным веществом, угнетающим центральную нервную систему человека.
Этиловый спирт также используется как топливо, в качестве растворителя, как наполнитель в спиртовых термометрах и как дезинфицирующее средство (или как компонент его).
- 1 Получение
- 1.1 Брожение
- 1.1.1 Промышленное производство спирта из биологического сырья
- 1.1.2 Гидролизное производство
- 1.2 Гидратация этилена
- 1.3 Очистка этанола
- 1.4 Абсолютный спирт
- 1.1 Брожение
- 2 Свойства
- 2.1 Физические свойства
- 2.2 Химические свойства
- 2.3 Пожароопасные свойства
- 3 Применение
- 3.1 Топливо
- 3.2 Химическая промышленность
- 3.3 Медицина
- 3.4 Парфюмерия и косметика
- 3.5 Пищевая промышленность
- 3.6 Прочее
- 4 Мировое производство этанола
- 5 Применение этанола в качестве автомобильного топлива
- 5.1 Автомобильный парк, работающий на этаноле
- 5.2 Экономичность
- 5.3 Экологические аспекты
- 6 Безопасность и регулирование
- 7 Действие этанола на организм человека
- 8 Виды и марки этанола
- 9 Этимология названий
- 9.1 Этимология термина «этанол»
- 9.2 Этимология названия «алкоголь»
- 9.3 Этимология слова «спирт»
- 10 Примечания
- 11 См. также
- 12 Ссылки
Получение
Существует 2 основных способа получения этанола - микробиологический (спиртовое брожение) и синтетический (гидратация этилена):
Брожение
См. также: Биоэтанол#БрожениеИзвестный с давних времён способ получения этанола - спиртовое брожение органических продуктов, содержащих углеводы (виноград, плоды и т. п.) под действием ферментов дрожжей и бактерий. Аналогично выглядит переработка крахмала, картофеля, риса, кукурузы, источником получения топливного спирта является вырабатываемый из тростника сахар-сырец и проч. Реакция эта довольно сложна, её схему можно выразить уравнением:
C6H12O6 → 2C2H5OH + 2CO2.
Раствор, получаемый в результате брожения, содержит не более 15 % этанола, так как в более концентрированных растворах дрожжи нежизнеспособны. Полученный таким образом этанол нуждается в очистке и концентрировании, обычно путем дистилляции.
Для получения этанола этим способом наиболее часто используют различные штаммы дрожжей вида Saccharomyces cerevisiae, в качестве питательной среды предварительно обработанные древесные опилки и/или раствор, полученный из них.
Промышленное производство спирта из биологического сырья
Современная промышленная технология получения этилового спирта из пищевого сырья включает следующие стадии:
- Подготовка и измельчение крахмалистого сырья - зерна (прежде всего - ржи, пшеницы), картофеля, кукурузы, яблок и т. п.
- Ферментация. На этой стадии происходит ферментативное расщепление крахмала до сбраживаемых сахаров. Для этих целей применяются рекомбинантные препараты альфа-амилазы, полученные биоинженерным путём - глюкамилаза, амилосубтилин.
- Брожение. Благодаря сбраживанию дрожжами сахаров происходит накопление в браге спирта.
- Брагоректификация. Осуществляется на разгонных колоннах.
Отходами бродильного производства являются углекислый газ, барда, эфиро-альдегидная фракция, сивушный спирт и сивушные масла.
Спирт, поступающий из брагоректификационной установки (БРУ) не является безводным, содержание этанола в нём до 95,6 %. зависимости от содержания в нём посторонних примесей, его разделяют на следующие категории:
- Альфа
- Экстра
- базис
- высшей очистки
- 1 сорт
Производительность современного спиртового завода около 30 000-100 000 литров спирта в сутки.
Гидролизное производство
Основные статьи: Гидролизный спирт , Гидролизное производствоВ промышленных масштабах этиловый спирт получают из сырья, содержащего целлюлозу (древесина, солома), которую предварительно гидролизуют. Образовавшуюся при этом смесь пентоз и гексоз подвергают спиртовому брожению. странах Западной Европы и Америки эта технология не получила распространения, но в СССР (ныне в России) существовала развитая промышленность кормовых гидролизных дрожжей и гидролизного этанола.
Гидратация этилена
В промышленности, наряду с первым способом, используют гидратацию этилена. Гидратацию можно вести по двум схемам:
- прямая гидратация при температуре 300 °C, давлении 7 МПа, в качестве катализатора применяют ортофосфорную кислоту, нанесённую на силикагель, активированный уголь или асбест:
- гидратация через стадию промежуточного эфира серной кислоты, с последующим его гидролизом (при температуре 80-90 °С и давлении 3,5 МПа):
Эта реакция осложняется образованием диэтилового эфира.
Очистка этанола
Этанол, полученный путём гидратации этилена или брожением, представляет собой водно-спиртовую смесь, содержащую примеси. Для его промышленного, пищевого и фармакопейного применения необходима очистка. Фракционная перегонка позволяет получить этанол с концентрацией около 95,6 % (мас.); эта неразделимая перегонкой азеотропная смесь содержит 4,4 % воды (мас.) и имеет температуру кипения 78,15 °C.
Перегонка освобождает этанол как от легколетучих, так и от тяжёлых фракций органических веществ (кубовый остаток).
Абсолютный спирт
Абсолютный спирт - этиловый спирт, практически не содержащий воды. Он кипит при температуре 78,39 °C, в то время как спирт-ректификат, содержащий не менее 4,43 % воды, кипит при 78,15 °C. Получают перегонкой водного спирта, содержащего бензол, и другими способами, например, спирт обрабатывают веществами, реагирующими с водой или поглощающими воду, такими как негашёная известь CaO или прокалённый медный купорос CuSO4.
Свойства
Физические свойства
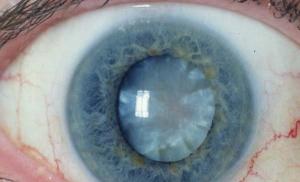
Внешний вид: в обычных условиях представляет собой бесцветную летучую жидкость с характерным запахом и жгучим вкусом. Этиловый спирт легче воды. Является хорошим растворителем других органических веществ. Следует избегать популярной ошибки: часто смешивают свойства 95,57 % спирта и абсолютизированного. Их свойства почти одинаковы, но величины начинают различаться, начиная с 3 - 4-й значащей цифры.
| Молекулярная масса | 46,069 а. е. м. |
| Температура плавления | −114,15 °C |
| Температура кипения | 78,39 °C |
| Критическая точка | 241 °C (при давлении 6,3 МПа) |
| Растворимость | смешивается с бензолом, водой, глицерином, диэтиловым эфиром, ацетоном, метанолом, уксусной кислотой, хлороформом |
| Показатель преломления | 1,3611
(температурный коэффициент показателя преломления 4,0·10−4, справедлив в интервале температур 10-30 °C) |
| Стандартная энтальпия образования ΔH | −234,8 кДж/моль (г) (при 298 К) |
| Стандартная энтропия образования S | 281,38 Дж/моль·K (г) (при 298 К) |
| Стандартная мольная теплоёмкость Cp | 1,197 Дж/моль·K (г) (при 298 К) |
| Энтальпия плавления ΔHпл | 4,81 кДж/моль |
| Энтальпия кипения ΔHкип | 839,3 кДж/моль |
Смесь 95,57 % этанола + 4,43 % воды является азеотропной, т. е. не разделяется при перегонке.
Химические свойства
Анимация трёхмерной модели молекулы этанолаТипичный представитель одноатомных спиртов.
Горюч. Легко воспламеняется. При достаточном доступе воздуха горит (за счёт его кислорода) светлым голубоватым пламенем, образуя терминальные продукты окисления - диоксид углерода и воду:
C2H5OH + 3O2 → 2CO2 + 3H2O
Ещё энергичнее эта реакция протекает в атмосфере чистого кислорода.
При определённых условиях (температура, давление, катализаторы) возможно и контролируемое окисление (как элементным кислородом, так и многими другими окислителями) до ацетальдегида, уксусной кислоты, щавелевой кислоты и некоторых других продуктов, например:
3C2H5OH + K2Cr2O7 + 4H2SO4 → 3CH3CHO + K2SO4 + Cr2(SO4)3 + 7H2O
Обладает слабо выраженными кислотными свойствами, в частности, подобно кислотам взаимодействует со щелочными металлами, а также магнием, алюминием и их гидридами, выделяя при этом водород и образуя солеподобные этилаты, являющиеся типичными представителями алкоголятов:
2C2H5OH + 2К → 2С2Н5ОК + Н2. C2H5OH + NaH → C2H5ONa + H2
Обратимо реагирует с карбоновыми и некоторыми неорганическими кислородсодержащими кислотами с образованием сложных эфиров:
С2Н5OH + RCOOH ⇄ RCOOС2Н5 + H2O С2Н5OH + HNO2 ⇄ С2Н5ONO + H2O
С галогеноводородами (HCl, HBr, HI) вступает в обратимые реакции нуклеофильного замещения:
C2H5OH + HX ⇄ C2H5X + H2O
Без катализаторов реакция с HCl идет относительно медленно; значительно быстрее - в присутствии хлорида цинка и некоторых других кислот Льюиса.
Вместо галогеноводородов для замещения гидроксильной группы на галоген могут быть использованы галогениды и галогеноксиды фосфора, тионилхлорид и некоторые другие реагенты, например:
3C2H5OH + PCl3 → 3C2H5Cl + H3PO3
Сам этанол также обладает нуклеофильными свойствами. частности, он относительно легко присоединяется по активированным кратным связям, например:
С2Н5OH + СH2=CНCN → С2Н5OСH2СH2CN,
реагирует с альдегидами с образованием полуацеталей и ацеталей:
RCHO + С2Н5OH → RCH(OH)OС2Н5 RCH(OH)OС2Н5 + С2Н5OH → RCH(OС2Н5)2 + H2O
При умеренном (не выше 120 °C) нагревании с концентрированной серной кислотой или другими водоотнимающими средствами кислотного характера образует диэтиловый эфир:
2С2Н5OH ⇄ С2Н5-O-С2Н5 + H2O
При более сильном нагревании с серной кислотой, а также при пропускании паров над нагретым до 350÷500 °C оксидом алюминия происходит более глубокая дегидратация. При этом образуется этилен:
CH3CH2OH ⇄ CH2=CH2 + H2O
При использовании катализаторов, содержащих наряду с оксидом алюминия высокодисперсное серебро и другие компоненты, процесс дегидратации может быть совмещён с контролируемым окислением этилена элементным кислородом, в результате чего с удовлетворительным выходом удается реализовать одностадийный процесс получения окиси этилена:
2CH3CH2OH +O2 → 2C2H4O + 2H2O
В присутствии катализатора, содержащего оксиды алюминя, кремния, цинка и магния, претерпевает серию сложных превращений с образованием в качестве основного продукта бутадиена (реакция Лебедева):
2C2H5OH → CH2=CH-CH=CH2 + H2O + H2
В 1932 году на основе этой реакции в СССР было организовано первое в мире крупнотоннажное производство синтетического каучука.
В слабощелочной среде образует иодоформ:
C2H5OH + 4I2 + 6NaHCO3 → CHI3 + HCOONa + 5NaI + 5H2O + 6CO2
Эта реакция имеет некоторое значение для качественного и количественного определения этанола в отсутствии других веществ, дающих подобную реакцию.
Пожароопасные свойства
Легковоспламеняющаяся бесцветная жидкость; давление насыщенного пара, кПа: lg p = 7.81158-1918.508/(252.125+t) при температуре от −31 до 78°С; теплота сгорания - 1408 кДж/моль; теплота образования -239,4 кДж/моль; температура вспышки 13°С (в закрытом тигле), 16°С (в открытом тигле); температура воспламенения 18°С; температура самовоспламенения 400°С; концентрационные пределы распространения пламени 3,6 - 17,7 % объёма; температурные пределы распространения пламени: нижний 11°С, верхний 41°С; минимальная флегматизирующая концентрация, % объёма: CO2 - 29.5, H2O - 35.7, N2 - 46; максимальное давление взрыва 682 кПа; максимальная скорость нарастания давления 15,8 МПа/с; скорость выгорания 0,037 кг/(м2 с); максимальная нормальная скорость распространения пламени - 0,556 м/с; минимальная энергия зажигания - 0,246 МДж; минимальное взрывоопасное содержание кислорода 11,1% объёма.
Применение
Топливо
Первым использовал этанол в качестве моторного топлива Генри Форд, который в 1880 г. создал первый автомобиль, работающий на этаноле. Возможность использования спиртов в качестве моторного топлива была показана также в 1902 г., когда на конкурсе в Париже были выставлены более 70 карбюраторных двигателей, работающих на этаноле и смесях этанола с бензином.
Этанол может использоваться как топливо, в т. ч. для ракетных двигателей (так, 70%-й водный этанол использовался в качестве топлива в первой в мире серийной баллистической ракете - немецкой «Фау-2»), двигателей внутреннего сгорания, бытовых, походных и лабораторных нагревательных приборов (т. н. "спиртовок"), грелок для туристов и военнослужащих (каталитическое автоокисление на платиновом катализаторе). Ограниченно (в силу своей гигроскопичности) используется в смеси с классическими нефтяными жидкими топливами. Применяется для выработки высококачественного топлива и компонента бензинов - Этил-трет-бутилового эфира, более независимого от ископаемой органики, чем МТБЭ.
Химическая промышленность
- служит сырьём для получения многих химических веществ, таких, как ацетальдегид, диэтиловый эфир, тетраэтилсвинец, уксусная кислота, хлороформ, этилацетат, этилен и др.;
- широко применяется как растворитель (в лакокрасочной промышленности, в производстве товаров бытовой химии и многих других областях);
- является компонентом антифризов и стеклоомывателей;
- в бытовой химии этанол применяется в чистящих и моющих средствах, в особенности для ухода за стеклом и сантехникой. Является растворителем для репеллентов.
Медицина
В медицине этиловый спирт в первую очередь используется как растворитель, экстрагент и антисептик. См. также: Медицинский антисептический раствор- по своему действию этиловый спирт можно отнести к антисептикам;
- как обеззараживающее и подсушивающее средство, наружно;
- подсушивающие и дубящие свойства 96%-го этилового спирта используются для обработки операционного поля или в некоторых методиках обработки рук хирурга;
- растворитель для лекарственных средств, для приготовления настоек, экстрактов из растительного сырья и др.;
- консервант настоек и экстрактов (минимальная концентрация 18 %);
- пеногаситель при подаче кислорода, искусственной вентиляции лёгких;
- в согревающих компрессах;
- для физического охлаждения при лихорадке (для растирания);
- компонент общей анестезии в ситуации дефицита медикаментозных средств;
- как пеногаситель при отёке лёгких в виде ингаляции 33 % раствора;
- этанол является противоядием при отравлении некоторыми токсичными спиртами, такими как метанол и этиленгликоль. Его действие обусловлено тем, что фермент алкогольдегидрогеназа, при наличии нескольких субстратов (например, метанол и этанол) осуществляет лишь конкурентное окисление, благодаря чему после своевременного (почти немедленного, вслед за метанолом/этиленгликолем) приёма этанола уменьшается текущая концентрация токсичных метаболитов (для метанола - формальдегида и муравьиной кислоты, для этиленгликоля - щавелевой кислоты).
Парфюмерия и косметика
Является универсальным растворителем различных веществ и основным компонентом духов, одеколонов, аэрозолей и т. п. Входит в состав разнообразных средств, включая даже такие как: зубные пасты, шампуни, средства для душа, и т. д.
Пищевая промышленность
Наряду с водой, является основным компонентом спиртных напитков (водка, вино, джин, пиво и др.). Также в небольших количествах содержится в ряде напитков, получаемых брожением, но не причисляемых к алкогольным (кефир, квас, кумыс, безалкогольное пиво и др.). Содержание этанола в свежем кефире ничтожно (0,12 %), но в долго стоявшем, особенно в тёплом месте, может достичь 1 %. кумысе содержится 1-3 % этанола (в крепком до 4,5 %), в квасе - от 0,5 до 1,2 %.
Растворитель для пищевых ароматизаторов. Может быть использован как консервант для хлебобулочных изделий, а также в кондитерской промышленности.
Зарегистрирован в качестве пищевой добавки E1510 .
Энергетическая ценность этанола - 7,1 ккал/г.
Прочее
Применяется для фиксирования и консервирования биологических препаратов.
Мировое производство этанола
Производство этанола по странам, млн литров. Данные ethanolrfa.org.
| Страна | 2004 | 2005 | 2006 | 2007 | 2008 | 2009 | 2010 |
|---|---|---|---|---|---|---|---|
| США | 13 362 | 16 117 | 19 946 | 24 565 | 34 776 | 40 068 | 45 360 |
| Бразилия | 15 078 | 15 978 | 16 977 | 18 972,58 | 24 464,9 | ||
| Евросоюз | - | - | - | 2 155,73 | 2 773 | ||
| Китай | 3 643 | 3 795 | 3 845 | 1 837,08 | 1 897,18 | ||
| Индия | 1 746 | 1 697 | 1 897 | 199,58 | 249,48 | ||
| Франция | 827 | 907 | 948 | - | - | ||
| Германия | 268 | 430 | 764 | - | - | ||
| Россия | 760 | 860 | 608 | 609 | 536 | 517 | 700 |
| ЮАР | 415 | 389 | 387 | - | - | ||
| Великобритания | 400 | 351 | 279 | - | - | ||
| Испания | 298 | 298 | 463 | - | - | ||
| Таиланд | 279 | 298 | 352 | 299,37 | 339,4 | ||
| Колумбия | - | - | 279 | 283,12 | 299,37 | ||
| Весь мир : | 40 710 | 45 927 | 50 989 | 49 524,42 | 65 527,05 |
Применение этанола в качестве автомобильного топлива
Основная статья: БиоэтанолТопливный этанол делится на биоэтанол и этанол, полученный другими методами (из отходов пластмасс, синтезированный из газа и т. п.).
Биоэтанол - это жидкое этанолсодержащее топливо, получаемое специальными заводами из крахмал-, целлюлозо- или сахаросодержащего сырья по системе укороченной дистилляции (позволяет получать качество, достаточное для использование в качестве топлива). Содержит метанол и сивушные масла, что делает его совершенно непригодным для питья. Применяется в чистом виде (точнее в виде азеотропа 96,6 %), а чаще в смеси с бензином (так называемый газохол) или дизельным топливом. Производство и использование биоэтанола увеличивается в большинстве стран мира, как более экологичная и возобновляемая альтернатива нефти.
Полноценно использовать биоэтанол способны лишь автомобили с соответствующим двигателем или с универсальным Flex-Fuel (способен потреблять смеси бензин/этанол с любым соотношением). Бензиновый двигатель способен потреблять бензин с добавкой этанола не более 30%, возможно также переоборудование обычного бензинового двигателя, но это экономически нецелесообразно.
Проблемой является недостаточная смешиваемость бензина и дизельного топлива с этанолом, из-за чего последний нередко выслаивается (при низких температурах всегда). Особенно эта проблема актуальна для России. Решения этой проблемы на данный момент не найдено.
Преимуществом смесей этанола с другими видами топлива перед «чистым» этанолом является лучшая зажигаемость, благодаря низкому содержанию влаги, тогда как «чистый» этанол (марка E100, с практическим содержанием C2H5OH 96,6 %) является неразделяемым дистилляцией азеотропом. Разделение же иными способами невыгодно. При добавлении этанола к бензину или дизелю происходит выслаивание воды.
В разных странах действуют следующие государственные программы применения этанола и содержащих его смесей на транспорте с двигателями внутреннего сгорания:
| Страна | Требования |
|---|---|
| Бразилия | 22-25 % этанола в бензине, 2% в дизельном топливе, доступны высокоэтанольные марки (E85, E100), их процент на рынке плавно увеличивают. Основной источник - сахарный тростник. Около 45 % мирового производства. |
| США | На США приходится 44,7 % мирового производства топливного спирта. Внедряются марки смеси этанола и бензина (E85, E10). Предполагается ввести 20% к 2020 году. |
| Венесуэла | 10% этанола в бензине. |
| Евросоюз | До ~6 % добавляется в обязательном порядке, внедряются этанольные марки E10 и выше. |
| Китай | Производить ежегодно 3 млн тонн к 2010 году/ |
| Аргентина | Обязательна 5% добавка этанола в любых марках бензина, внедряются марки с большим содержанием. |
| Таиланд | 5 % этанола является минимальным допустимым содержанием в бензине. |
| Украина | Законодательно установлено содержание 5% этанола в бензине с 2013, и 7% с 2014 года. На заправках широко продается топливо с содержанием биоэтанола в от 30 до 37,2% |
| Колумбия | 10%-я смесь в больших городах к сентябрю 2005 года/ |
| Канада | 5%-я смесь с сентября 2010 года |
| Япония | Разрешено 3%-е содержание этанола в бензине и менее. |
| Индия | 20 % биотоплив к 2017 году. Сейчас 5 %. Производится из самого различного сырья, в частности из древесной стружки. |
| Австралия | Этанола в бензине не более 10 %, марка E10. |
| Индонезия | 10 % спирта в бензине/ |
| Филиппины | E10 постепенно внедряется. |
| Ирландия | Марки E5-E10 достаточно широко применяются и продолжат внедряться. |
| Дания | Аналогично Ирландии. |
| Чили | Разрешено 2 % содержание этанола в автомобильном топливе. |
| Мексика | 3,2 % биотоплив в автомобильном топливе к 2012 году обязательно. Америке самая неохотно внедряющая биотопливо страна. |
В США «Энергетический билль», подписанный президентом Бушем в августе 2005 года, предусматривает производство к 2012 году ежегодно 30 миллиардов литров этанола из зерна и 3,8 миллиардов литров из целлюлозы (стебли кукурузы, рисовая солома, отходы лесной промышленности).
Внедрение производства биотоплива является затратным процессом, однако дает экономике преимущества впоследствии. Так например, строительство завода по производству этанола мощностью 40 млн галлонов даёт экономике (на примере США):
- 142 млн долл. инвестиций во время строительства;
- 41 рабочее место на заводе, плюс 694 рабочих места во всей экономике;
- Увеличивает местные цены на зерновые на 5-10 центов за бушель;
- Увеличивает доходы местных домохозяйств на 19,6 млн долл. ежегодно;
- Приносит в среднем 1,2 млн долларов налогов;
- Доходность инвестиций 13,3 % годовых.
В 2006 г. этаноловая индустрия дала экономике США:
- 160231 новых рабочих мест во всех секторах, включая 20000 рабочих мест в строительстве;
- Увеличила доходы домохозяйств на $6,7 миллиарда;
- Принесла $2,7 млрд федеральных налогов и $2,3 млрд местных налогов.
В 2006 году в США было переработано в этанол 2,15 миллиарда бушелей кукурузы, что составляет 20,5 % годового производства кукурузы. Этанол стал третьим по величине потребителем кукурузы после животноводства и экспорта. На этанол перерабатывается 15 % урожая сорго США.
Производство барды этаноловой промышленностью США, метрических тонн в сухом весе.
Барда является вторичным кормовым сырьём, а также может быть использована для получения биогаза.
Автомобильный парк, работающий на этаноле
Смесь этанола с бензином обозначается буквой Е. Цифрой у буквы Е обозначается процентное содержание этанола. Е85 - означает смесь из 85 % этанола и 15 % бензина.
Смеси до 20 % содержания этанола могут применяться на любом автомобиле. Однако некоторые производители автомобилей ограничивают гарантию при использовании смеси с содержанием более 10 % этанола. Смеси, содержащие более 20 % этанола, во многих случаях требуют внесения изменения в систему зажигания автомобиля.
Автопроизводители выпускают автомобили, способные работать и на бензине, и на Е85. Такие автомобили называются «Flex-Fuel». Бразилии такие автомобили называют «гибридными». русском языке названия нет. Большинство современных автомобилей либо изначально поддерживают использование такого топлива, либо опционально, по соответствующему запросу.
В 2005 году в США более 5 млн автомобилей имели гибридные двигатели. конце 2006 г. в США эксплуатировалось 6 млн автомобилей с такими двигателями. Общий автопарк составляет 230 млн автомобилей.
1200 заправочных станций продают Е85 (май 2007). Всего в США автомобильное топливо продают около 170 000 заправочных станций.
Экономичность
Себестоимость бразильского этанола (около 0,19 долларов США за литр в 2006 г.) делает его использование экономически выгодным.
Экологические аспекты
Биоэтанол как топливо часто называют «нейтральным» в качестве источника парниковых газов. Он обладает нулевым балансом диоксида углерода, поскольку при его производстве путём брожения и последующем сгорании выделяется столько же CO2, сколько до этого было взято из атмосферы использованными для его производства растениями. Однако, ректификация этанола требует дополнительных затрат энергии, вырабатываемой одним из «традиционных» способов (в т. ч. и сжиганием ископаемого топлива).
В 2006 году применение этанола в США позволило сократить выбросы около 8 млн тонн парниковых газов (в СО2 эквиваленте), что примерно равно годовым выхлопам 1,21 млн автомобилей.
Безопасность и регулирование
Денатурат- Этанол - горючее вещество, смесь его паров с воздухом взрывоопасна.
- Спирт этиловый синтетический, технический и пищевой, непригодный для производства алкогольной продукции, входит в список ядовитых веществ для целей статьи 234 и других статей Уголовного кодекса Российской Федерации.
- С 2005 года розничная продажа спирта в России запрещена (за исключением районов Крайнего Севера).
Действие этанола на организм человека
Основные статьи: Токсикология этанола , АлкоголизмЭтанол в алкогольных напитках - канцероген с доказанной способностью вызывать рак. зависимости от дозы, концентрации, пути попадания в организм и длительности воздействия этанол также может обладать наркотическим и токсическим действием. Под наркотическим действием обозначается его способность вызвать кому, ступор, нечувствительность к боли, угнетение функций ЦНС, алкогольное возбуждение, привыкание, а также его наркозное действие. Под действием этанола происходит выделение эндорфинов в прилежащем ядре (Nucleus accumbens), у страдающих алкоголизмом также в орбитофронтальной коре (поле 10). Тем не менее, с юридической точки зрения этиловый спирт наркотиком не признан, так как это вещество не включено в международный список контролируемых веществ конвенции ООН 1988 года. определённых дозах к массе тела и концентрациях приводит к острому отравлению и смерти (смертельная разовая доза - 4-12 граммов этанола на килограмм массы тела).
Основной метаболит этанола ацетальдегид является токсичным, мутагенным и канцерогенным веществом. Существуют доказательства канцерогенности ацетальдегида в экспериментах на животных; кроме того, ацетальдегид повреждает ДНК.
Длительное употребление этанола может вызвать такие заболевания, как цирроз печени, гастрит, язва желудка, рак желудка и рак пищевода, сердечно-сосудистые заболевания.
Употребление этанола может вызвать оксидативное повреждение нейронов головного мозга, а также их гибель вследствие повреждения гемато-энцефалического барьера.
Злоупотребление алкогольными напитками может привести к клинической депрессии и алкоголизму.
Этанол является естественным метаболитом человеческого организма и может в небольших количествах синтезироваться в тканях организма (истинный эндогенный алкоголь) или в желудочно-кишечном тракте в результате процессов ферментации углеводной пищи (условный эндогенный алкоголь). Количество эндогенного алкоголя редко превышает 0,18 промилле, что находится на границе чувствительности самых современных приборов. Обычный алкотестер такие количества определить не может.
Виды и марки этанола
- Ректификат (точнее, спирт-ректификат) - это очищенный путём ректификации этиловый спирт, содержит 95,57 %, химическая формула C2H5OH. Может выпускаться по ГОСТ 18300-72 (Госстандарт СССР, спирт этиловый ректификованный технический, технические условия) и ГОСТ 5964-82; ГОСТ 5964-93. зависимости от степени очистки технический этиловый ректификованный спирт выпускают марки «Экстра» и двух сортов: высшего и первого
- Спирт этиловый абсолютированный - содержание спирта >99,9 %.
- Спирт медицинский - содержание спирта 96,4-96,7%.
Этимология названий
Для обозначения данного вещества используется несколько наименований. Технически наиболее правильным является термин этанол или этиловый спирт. Однако значительное распространение получили названия алкоголь, винный спирт или просто спирт, хотя спирты, или алкоголи - это более широкий класс веществ.
Этимология термина «этанол»
Названия этанол и этиловый спирт указывают на то, что данное соединение содержит в своей основе этил - радикал этана. При этом слово спирт (суффикс -ол) в названии указывает на содержание гидроксильной группы (-OH), характерной для спиртов.
Этимология названия «алкоголь»
Название алкоголь происходит от араб. الكحل аль-кухуль, означающего мелкий порошок, полученный возгонкой, порошкообразная сурьма, порошок для подкрашивания век.
В русский язык слово «алкоголь» пришло через его немецкий вариант нем. alkohol. Однако в русском языке сохранился в виде архаизма, по всей видимости, и омоним слова «алкоголь» в значении «мелкий порошок».
Этимология слова «спирт»
Наименование этанола винный спирт произошло от лат. spiritus vini (дух вина). русский язык слово «спирт» пришло через английский его вариант англ. spirit.
В английском языке слово «спирт» в данном значении использовалось уже в середине XIII века, и только начиная с 1610 года слово «спирт» стало употребляться алхимиками для обозначения летучих веществ, что соответствует основному значению слова «spiritus» (испарения) в латинском языке. К 1670-м годам значение слова сузилось до «жидкостей с высоким процентным содержанием алкоголя», а летучие жидкости получили название эфиров.
См. также Этимология названия в статье «Спирты».
Примечания
- European chemical Substances Information System Проверено 8 декабря 2013.
- Chastain G (2006). «Alcohol, neurotransmitter systems, and behavior». The Journal of general psychology 133 (4). DOI:10.3200/GENP.133.4.329-335. PMID 17128954.
- Статья «Абсолютный спирт» в БСЭ.
- Получение абсолютного спирта
- Этиловый спирт: химические и физические свойства
- В.Г.Козин, Н.Л.Солодова, Н.Ю.Башкирцева, А.И.Абдуллин. Современные технологии производства компонентов моторных топлив. Учебное пособие. - Казань: КГТУ, 2009. - 327 с.
- Средства, влияющие на ЦНС
- Flomenbaum, Goldfrank et al. Goldfrank"s Toxicologic Emergencies. 8th Edition. - McGraw Hill, 2006. - С. 1465. - 2170 с. - ISBN 0071437630.
- Федеральное агентство по техническому регулированию и метрологии. ГОСТ Р 52409-2005 (полный текст)
- Russell, Nicholas J. Food preservatives. - New York: Kluwer Academic/Plenum Publishers, 2003. - P. 198. - ISBN 0-306-47736-X.
- E1510 - спирт этиловый
- 2008 Ethanol Production Exceeds 9 Billion Gallons
- Ethanol World Production Statistics
- Национальная Программа.рф - Альтернативные виды топлива
- 1 2 Биоэтанол: обзор мирового и российского рынков. Cleandex.
- Информационно аналитическое агентство «ИНФОБИО»
- ЭКОТОК
- 1 2 Россия и Америка в XXI веке
- Евросоюз с 1 января отказывается от традиционного бензина /16.12.2010
- биоэтанол, биобензин, альтернативное топливо INNOVATIVE Е 95 проблема использования применения
- Ottawa to push ethanol, despite concerns (недоступная ссылка с 23-05-2013 (793 дня) - история, копия)
- Интерфакс Запад
- India Sets Target of 20 % Biofuels by 2017
- Ivan Castano Mexican Biofuels Seen Meeting 3 % Blending Target In 2012 2 Май 2011
- Национальная Биотопливная Ассоциация
Спирт и алкоголь достаточно плотно вошли в нашу повседневную жизнь. В этой статье будут даны основные рекомендации относительно того, как отличить метиловый от Также будут указаны их характеристики и химические формулы.
История открытия спирта
Формула спирта в том или ином виде была открыта практически одновременно во многих регионах земного шара. В 1334 году французский алхимик Арно де Вильггер изначально получил винный спирт. В 1360 году итальянские и французские монастыри производили такое вещество под названием «вода жизни». Генуэзские купцы в 1386 году привезли спирт в Москву, чтобы продемонстрировать его качества.
Определение
Теперь разберемся с тем, что такое этиловый и метиловый спирт.
Помните, что если вы превысите норму, то алкоголь станет ядом, который нанесет вред органам и даже целым системам вашего организма.
Собственно на этом и можно закончить рассуждение о том, как отличить метиловый от этилового спирта.
Сегодня реалии таковы, что этиловый спирт занимает ведущее место среди продуктов органического синтеза. Он используется и в косметологии, и в медицине.
Кроме того, спирт используется в производстве . Со времен школы известно, что C 2 H 5 OH — это формула спирта, но не все знают, как на самом деле его производят.
Способы производства
Первый вариант получения этилового спирта - спиртовое брожение. Этот способ известен еще с незапамятных времен. Если не вдаваться в подробности, то брожение происходит за счет жизнедеятельности бактерий и дрожжей. В качестве сырья обычно используют виноград, так как в своем составе он содержит углеводы и сахарозу. Таким же методом перерабатываются кукуруза, рис, картофель.
После брожения концентрация в растворе C 2 H 5 OH (химическая формула этилового спирта) достигает 15%. Такой низкий процент объясняется тем, что при большей концентрации дрожжи начинают погибать в собственном спиртовом растворе. Далее путем дистилляции этанол концентрируют, а так же очищают.
На производстве спирта из пищевого сырья выделяют следующие этапы:
- кукуруза, пшеница, картофель, зерна ржи подвергаются измельчению;
- расщепление крахмала на сахара (ферментация);
- накопление спирта за счет брожения при помощи дрожжей сахара;
- очистка и фильтрация полученного раствора (ректификация).
После прохождения всех этапов концентрация этанола становится 95,6%.

Промышленное производство
Древесина, солома, содержащие целлюлозу, используются в промышленности для получения этилового спирта. Целлюлозу подвергают гидролизу, то есть происходит процесс разложения составляющих раствора при помощи воды для получения новых образований. Химическая формула спирта, полученного путем гидратации выглядит так:
CH 2 =CH 2 + H 2 O -> C 2 H 5 OH
В процессе переработки сырья в этаноле образуются различные примеси. Для применения в промышленной, фармакологической и пищевой отраслях, требуется его очистка.
Ректификация спирта - так называется процесс химической очистки этанола от вредных примесей. После нее пропадает характерный неприятный запах сивушных масел. Его формула остается неизменной, но он становится прозрачным, потому как не содержит посторонних частиц. Более высокую крепость и сорт имеет спирт, очищенный лучше и качественнее (ректификация проводится несколько раз). Питьевым является спирт-ректификат, прошедший высшую степень очистки.
Этиловый спирт или винный является широко распространённым представителем спиртов. Известно много веществ, в состав которых наряду с углеродом и водородом входит кислород. Из числа кислородсодержащих соединений мне интересен прежде всего класс спиртов.
Этиловый спирт
Физические свойства спирта . Этиловый спирт С 2 Н 6 О - бесцветная жидкость со своеобразным запахом, легче воды (удельный вес 0,8), кипит при температуре 78°,3, хорошо растворяет многие неорганические и органические вещества. Спирт «ректификат» содержит 96% этилового спирта и 4% воды.
Строение молекулы спирта .Согласно валентности элементов, формуле С 2 Н 6 О соответствуют две структуры:
Чтобы решить вопрос о том, какая из формул соответствует спирту в действительности, обратимся к опыту.
Поместим в пробирку со спиртом кусочек натрия. Тотчас начнётся реакция, сопровождающаяся выделением газа. Нетрудно установить, что этот газ - водород.
Теперь поставим опыт так, чтобы можно было определить, сколько атомов водорода выделяется при реакции из каждой молекулы спирта. Для этого в колбу с мелкими кусочками натрия (рис. 1) прибавим по каплям из воронки определённое количество спирта, например 0,1 грамм-молекулы (4,6 грамма). Выделяющийся из спирта водород вытесняет воду из двугорлой склянки в измерительный цилиндр. Объём вытесненной воды в цилиндре соответствует объёму выделившегося водорода.

Рис.1. Количественный опыт получения водорода из этилового спирта.
Так как для опыта была взята 0,1 грамм-молекулы спирта, то водорода удаётся получить (в пересчёте на нормальные условия) около 1,12 литра. Это означает, что из грамм-молекулы спирта натрий вытесняет 11,2 литра , т.е. половину грамм-молекулы, иначе говоря 1 грамм-атом водорода. Следовательно, из каждой молекулы спирта натрием вытесняется только один атом водорода.
Очевидно, в молекуле спирта этот атом водорода находится в особом положении по сравнению с остальными пятью атомами водорода. Формула (1) не даёт объяснения такому факту. Согласно ей, все атомы водорода одинаково связаны с атомами углерода и, как нам известно, не вытесняются металлическим натрием (натрий хранят в смеси углеводородов - в керосине). Наоборот, формула (2) отражает наличие одного атома, находящегося в особом положении: он соединён с углеродом через атом кислорода. Можно заключить, что именно этот атом водорода связан с атомом кислорода менее прочно; он оказывается более подвижным и вытесняется натрием. Следовательно, структурная формула этилового спирта:

Несмотря на большую подвижность атома водорода гидроксильной группы по сравнению с другими атомами водорода, этиловый спирт не является электролитом и в водном растворе не диссоциирует на ионы.

Чтобы подчеркнуть, что в молекуле спирта содержится гидроксильная группа - ОН, соединённая с углеводородным радикалом, молекулярную формулу этилового спирта пишут так:

Химические свойства спирта . Выше мы видели, что этиловый спирт реагирует с натрием. Зная строение спирта, мы можем эту реакцию выразить уравнением:

Продукт замещения водорода в спирте натрием носит название этилата натрия. Он может быть выделен после реакции (путём испарения избытка спирта) в виде твёрдого вещества.
При поджигании на воздухе спирт горит синеватым, еле заметным пламенем, выделяя много тепла:

Если в колбе с холодильником нагревать этиловый спирт с галогеноводородной кислотой, например с НВг (или смесью NаВг и Н 2 SО 4 , дающей при реакции бромистый водород), то будет отгоняться маслянистая жидкость - бромистый этил С 2 Н 5 Вг:

Эта реакция подтверждает наличие гидроксильной группы в молекуле спирта.
При нагревании с концентрированной серной кислотой в качестве катализатора спирт легко дегидратируется, т. е. отщепляет воду (приставка «де» указывает на отделение чего-либо):

Эта реакция используется для получения этилена в лаборатории. При более слабом нагревании спирта с серной кислотой (не выше 140°) каждая молекула воды отщепляется от двух молекул спирта, вследствие чего образуется диэтиловый эфир - летучая легко воспламеняющаяся жидкость:
Диэтиловый эфир (иногда называемый серным эфиром) применяется в качестве растворителя (чистка тканей) и в медицине для наркоза. Он относится к классу простых эфиров - органических веществ, молекулы которых состоят из двух углеводородных радикалов, соединённых посредством атома кислорода: R - О - R1
Применение этилового спирта . Этиловый спирт имеет большое практическое значение. Много этилового спирта расходуется на получение синтетического каучука по способу академика С. В. Лебедева. Пропуская пары этилового спирта через специальный катализатор, получают дивинил:
который затем может полимеризоваться в каучук.
Спирт идёт на выработку красителей, диэтилового эфира, различных «фруктовых эссенций» и ряда других органических веществ. Спирт как растворитель применяется для изготовления парфюмерных продуктов, многих лекарств. Растворяя в спирте смолы, готовят различные лаки. Высокая теплотворная способность спирта обусловливает применение его в качестве горючего (автомобильного топлива = этанола).
Получение этилового спирта . Мировое производство спирта измеряется миллионами тонн в год.
Распространённым способом получения спирта является брожение сахаристых веществ в присутствии дрожжей. В этих низших растительных организмах (грибках) вырабатываются особые вещества - ферменты, которые служат биологическими катализаторами реакции брожения.
В качестве исходных материалов в производстве спирта берут семена злаков или клубни картофеля, богатые крахмалом. Крахмал с помощью солода, содержащего фермент диастаз, сперва превращают в сахар, который затем сбраживают в спирт.
Учёные много работали над тем, чтобы заменить пищевое сырьё для получения спирта более дешёвым непищевым сырьём. Эти поиски увенчались успехом.
В последнее время в связи с тем, что при крекинге нефти образуется много этилена, стали
Реакция гидратации этилена (в присутствии серной кислоты) была изучена ещё А. М. Бутлеровым и В. Горяиновым (1873), который предсказал и её промышленное значение. Разработан и внедрен в промышленность также метод прямой гидратации этилена пропусканием его в смеси с парами воды над твердыми катализаторами. Получение спирта из этилена очень экономично, так как этилен входит в состав газов крекинга нефти и других промышленных газов и, следовательно, является широкодоступным сырьем.
Другой способ основан на использовании в качестве исходного продукта ацетилена. Ацетилен подвергается гидратации по реакции Кучерова, а образующийся уксусный альдегид каталитически восстанавливают водородом в присутствии никеля в этиловый спирт. Весь процесс гидратации ацетилена с последующим восстановлением водородом на никелевом катализаторе в этиловый спирт может быть представлен схемой.
Гомологический ряд спиртов
Кроме этилового спирта, известны и другие спирты, сходные с ним по строению и свойствам. Все они могут рассматриваться как производные соответствующих предельных углеводородов, в молекулах которых один атом водорода заменён гидроксильной группой:
Таблица
|
Углеводороды |
Спирты |
Температура кипения спиртов в º С |
| Метан СН 4 | Метиловый СН 3 ОН | 64,7 |
| Этан С 2 Н 6 | Этиловый С 2 Н 5 ОН илиСН 3 - СН 2 - ОН | 78,3 |
| Пропан С 3 Н 8 | Пропиловый С 4 Н 7 ОН или СН 3 - СН 2 - СН 2 - ОН | 97,8 |
| Бутан С 4 Н 10 | Бутиловый С 4 Н 9 ОН илиСН 3 - СН 2 - СН 2 - ОН | 117 |
Будучи сходны по химическим свойствам и отличаясь друг от друга по составу молекул на группу атомов СН 2 , эти спирты составляют гомологический ряд. Сравнивая физические свойства спиртов, мы в этом ряду, так же как и в ряду углеводородов, наблюдаем переход количественных изменений в изменения качественные. Общая формула спиртов данного ряда R - ОН (где R - углеводородный радикал).
Известны спирты, в молекулы которых входит несколько гидроксильных групп, например:

Группы атомов, обусловливающие характерные химические свойства соединений, т. е. их химическую функцию, называются функциональными группами.
Спиртами называются органические вещества, молекулы которых содержат одну или несколько функциональных гидроксильных групп, соединённых с углеводородным радикалом .
По своему составу спирты отличаются от углеводородов, соответствующих им по числу углеродных атомов, наличием кислорода (например, С 2 Н 6 и С 2 Н 6 О или С 2 Н 5 ОН). Поэтому спирты можно рассматривать как продукты частичного окисления углеводородов.
Генетическая связь между углеводородами и спиртами
Произвести непосредственное окисление углеводорода в спирт довольно трудно. Практически проще это сделать через галогенопроизводное углеводорода. Например, чтобы получить этиловый спирт, исходя из этана С 2 Н 6 , можно сначала получить бромистый этил по реакции:
а затем бромистый этил превратить в спирт нагреванием с водой в присутствии щёлочи:
Щёлочь при этом нужна, чтобы нейтрализовать образующийся бромистый водород и устранить возможность реакции его со спиртом, т.е. сдвинуть эту обратимую реакцию вправо.
Подобным же образом метиловый спирт может быть получен по схеме:
Таким образом, углеводороды, их галогенопроизводные и спирты находятся между собой в генетической связи (связи по происхождению).
Не является секретом то, что в качестве основного сырья для производства водочных изделий служит спирт этиловый ректификованный. Это немалозначимый продукт в указанной сфере. Об этом подробнее далее.
Описание материала
Ректификованный собой представляет бесцветную прозрачную жидкость, которая не обладает посторонними запахами и привкусами. данного продукта при 20 °С равняется 0,78927 г/см3. Этанол, или этиловый спирт, впервые был синтезирован в 1855 г. из этилена. Данное вещество является легковоспламеняющейся жидкостью. При его горении образуется вода и диоксид углерода. Пары спирта являются вредными для здоровья. Предельной допустимой нормой его концентрации в воздухе считается 1 мг/дм³. Температура его замерзания составляет -117 °С, а кипения: +78,2 °С.
Этиловый спирт - формула
Это немаловажно знать. Общая химическая формула этилового спирта: С 2 -Н 5 -ОН. Она выражает состав продукта и была установлена еще 1807 году. Но только после того, как удалось синтезировать этиловый спирт, формула была выведена структурная. Она пишется следующим образом: СН 3 СН 2 ОН.
Этанол является насыщенным спиртом и, так как он содержит лишь одну группу ОН, относится к категории одноатомных. Наличие гидроксильной группы определяет химические свойства вещества, а также реакционную слабость данного продукта.
При хранении в негерметичных емкостях происходит испарение этилового спирта, а также поглощается влага из воздуха. Это происходит в результате того, что этанол относится к гигроскопичным веществам. В связи с тем что указанный продукт обладает структурой, близкой к воде, он может смешиваться с ней в любых соотношениях.
Ректификованный, полученный в промышленных условиях, имеет слабокислую реакцию. Это достоверный факт. Он в незначительном количестве содержит органические кислоты. Реакция же химически чистого этилового спирта нейтральная. Это следует помнить.
Требования, которые предъявляются к качеству зерна
Главной задачей, стоящей перед изготовителями алкогольной продукции, является получение этилового спирта высшего качества. Государственными стандартам и другими нормативными документами к этому предъявляются высокие требования, которые затрагивают физико-химические и органолептические показатели. Этиловый спирт получают из различного природного сырья.

Изготовление указанного вещества из сельскохозяйственного сырья является биотехническим производством, которое использует микроорганизмы для превращения крахмала в сбраживаемые сахара, а затем в готовый материал - этанол. Все этапы от приемки зерна до ректификации содержат большое количество химических и механических процессов. Каждый из них сказывается на органолептических показателях этилового спирта. Об этом будет рассказано далее.
Факторы, влияющие на органолептические показатели
В данном случае это:
- Санитарное состояние оборудования на производстве (трубопроводов, испарительной камеры, теплообменников, передаточного чана).
- Качество сырья (вид зерна, условия его хранения, состояние, запах и др.).
- Используемая подготовки сырья (механико-ферментативная, традиционная).
- Способ обработки (степень помола, на складе, в производстве).
- Используемые виды дрожжей.
- Протекание процесса сбраживания (продолжительность, нарастание кислотности).
- Используемые вспомогательные материалы (антисептики и дезинфицирующие средства).
Одним из самых главных факторов является качество используемого сырья. Положение с ним достаточно сложное, так как государственных поставок зерна нет. Поэтому основная часть используемого сырья доставляется на предприятия по контрактам. Они заключаются с различными поставщиками по договорным ценам.
На сегодняшний день не существует государственного стандарта или иной нормативно-технической документации, которая бы четко определяла все требования к зерну, используемому для изготовления указанного продукта. Однако некоторые из них закреплены в «Регламенте на производство спирта из крахмалосодержащего сырья». Среди них - содержание различных токсичных примесей (семян, сорняков и т. д.), зараженность вредителями злаков, а также установление сорности.
Применение спиртов в изготовлении алкогольных напитков требует высокого качества получаемого продукта. От состояния используемого зерна напрямую зависят органолептические свойства получаемого из него указанного вещества. Наиболее существенным показателем сырья является его запах. Благодаря капиллярно-пористой структуре зерна и скважистости соответствующей массы оно способно сорбировать (поглощать) различные газы и пары из окружающей среды. То сырье, которое заражено амбарными вредителями, может содержать и продукты их жизнедеятельности. Если в зерне присутствуют клещи, то ухудшается его цвет и вкус, а также образуется специфический неприятный запах. Повреждение оболочки данного сырья создает благоприятные условия для развития микроорганизмов и накоплению микотоксинов. Использовать такое зерно для производства можно. Однако наличие значительного числа насекомых отрицательно сказывается на органолептических показателях полученного спирта.
Для изготовления указанного продукта часто используется некачественное и дефектное зерно, среди которого недозрелое и свежеубранное, поврежденное сушкой, подвергнутое самонагреванию, пораженное спорыньей и головней, а также фузариозом. Это достоверный факт. При переработке свежеубранного зерна без выдержки для дозревания происходит нарушение технологии, которое приводит к затруднению бражки и, как следствие, значительному снижению производительности соответствующего отделения.
Цвет данного сырья, поврежденного сушкой, может измениться от светло-коричневого до черного. Это важно знать. Зерно черного цвета относят к сорной примеси. В результате этого перерабатывают его, только смешивая со здоровым. При этом допустимая норма горелых зерен не должна быть более 10%. Применение спиртов для производства водочной продукции высокого качества при превышении этого показателя недопустимо.
Сырье, зараженное спорыньей и головней, становится токсичным, так как содержит различные алкалоиды (аргонин, эрготамин, кортунин и др). Вредные примеси являются весьма нежелательными, так как они влияют на органолептические показатели спирта и придают ему резкость, горечь и жгучесть. Однако данное сырье можно перерабатывать в смеси со здоровым зерном. При этом его содержание не должно быть более 8-10%.
Зерно, которое используется для производства спирта, состоит из крахмала (65 - 68% на абсолютно сухое вещество), а также белка, жиров, свободных сахаров, минеральных элементов, полисахаридов, декстрина. Все перечисленные соединения на разных стадиях осуществления технологического процесса участвуют в различных биохимических реакциях.
Еще одним фактором, который влияет на органолептические свойства готовой продукции, является солод и ферментные препараты микроорганизменных культур (осахаривающие материалы). Это следует также учесть. Достаточно часто на производстве могут использоваться инфицированные указанные препараты. Также бывает, что они поступают с недостаточной ферментативной активностью. В таком случае происходит инфицированный процесс сбраживания. В результате этого происходит накапливание нежелательных продуктов жизнедеятельности дрожжей. Поэтому окисляемость спирта снижается. Из-за этого ухудшается его запах и вкус.
Качество получаемого спирта непосредственно зависит от различных используемых типов дрожжей. Их правильный выбор, а также грамотное определение параметров их сбраживания позволяет получить указанный продукт, обладающий низким содержанием основных примесей.

Также важным компонентом при производстве спирта является вода. От ее чистоты (количества присутствующих микроорганизмов, а также различных растворенных в ней химических веществ) зависит качество производимого продукта. Лучше всего использовать воду, поступающую из артезианских источников.
Также следует учесть, что после очистки в указанном продукте остаются различные токсичные примеси. Высшие эфиры, иногда присутствующие в произведенном спирте, могут придавать легкий, едва заметный фруктовый запах. Это достоверный факт. А вот наличие диэтилового эфира придает указанному продукту горечь и гнилостный запах.
На качество данного вещества и его органолептические показатели также влияют различные нетипичные примеси, микробные и иные токсины, пестициды и др.
Технология получения спирта
Данный пункт рассмотрим подробнее. Спирт этиловый ректификованный можно изготовить тремя способами: химическим, синтетическим и биохимическим (ферментативным). Их выбор зависит от индивидуального подхода.

Пищевой спирт этиловый ректификованный получают исключительно из соответствующего сырья. В основном для этого служат зерно, патока и картофель. Спирт этиловый ректификованный технический получают из этого же сырья. Однако он может содержать различные примеси, которые непозволительны для пищевой промышленности.
Производство этилового спирта осуществляют в 3 этапа

Одним из лучших видов растительного сырья, которое используется для производства указанного продукта, является картофель. Для этого используются такие его сорта, которые обладают высокой крахмалистостью, а также весьма устойчивы при хранении. Это является важным условием при производстве.
Также следует знать, что зерно используют не только как сырье, но и для получения солода, который является источником ферментов, расщепляющих крахмал до сбраживающих сахаров. Это зависит от индивидуального желания. На некоторых заводах вместо солода используются ферментативные препараты микробного происхождения. Получают их из плесневых грибов. Препараты ферментные могут являться полной заменой солоду либо использоваться совместно с ним в различных соотношениях.
Свойства спиртов определяют технологию производства. В сырце содержится ряд примесей, которые различаются по температуре кипения. Они являются побочными продуктами при брожении. Их остаточное количество и состав влияют на качество получаемого спирта и производимых ликероводочных изделий. Это существенный факт.
Необходимое оборудование
Для получения указанного продукта из спирта-сырца используют многоколонные установки. Их применение является немаловажным. Каждая колонна указанной установки осуществляет конкретную функцию разделения соответствующей смеси при различных температурах и давлении. Реакции спиртов и их физико-химические свойства позволяют избавиться от различных примесей. Это имеет большое значение в данном случае. Они недопустимы при производстве пищевого спирта. В настоящее время существуют несколько новых запатентованных технологических схем очистки и производства сырья, которые позволяют значительно повысить аналитические и органолептические показатели указанного продукта. Производительность брагоректификации при этом повышается на 15%. Выход же окончательного продукта приближается к 98,5%. На сегодняшний день на производстве указанного вещества применяют брагоректификационные установки непрерывного действия, которые могут содержать до пяти колонн. Они бывают различными и, в соответствии со своим назначением, подразделяются на:

Глубокая очистка
Ректификация - это своеобразная многоступенчатая перегонка. Она осуществляется в колоннах при помощи пара и многоколпачковых тарелок. На этих установках получают указанное вещество, а также легколетучие компоненты и сивушное масло, которое является смесью высших спиртов. В соответствии с процессом ректификации эти примеси подразделяются на:
- Хвостовые. К ним принято относить те элементы, температура кипения которых выше, чем у этилового спирта. Это а также другие вещества. Например, фурфурол, ацетали и др.
- Головные. К ним относят примеси, которые кипят при температуре меньшей, чем этиловый спирт. В данном случае это эфиры и альдегиды.
- Промежуточные примеси и предельные спирты. Они являются наиболее трудноотделимыми группами соединений. В зависимости от различных условий осуществления перегонки они могут быть как хвостовыми, так и головными.
Разновидности
В зависимости от степени очистки указанный продукт подразделяется на:
- 1 сорт. Этот этиловый спирт применение нашел в медицине. Однако для производства алкогольных напитков он не используется.
- «Люкс».
- «Экстра».
- «Базис».
- «Альфа».
Для изготовления водочной продукции, которая по качеству будет соответствовать всем современным требованиям, нужно использовать спирт с отсутствием примесей токсичного характера. Он должен отвечать требованиям, указанным в ГОСТ Р 51652—2000.

Этиловый спирт - применение
В этом плане все довольно просто и понятно. Применение спиртов весьма разнообразно. Однако чаще всего их используют в медицинских целях, для производства алкогольной продукции, а также в промышленности.
Особенности изготовления
Разные виды указанного вещества получают из различного сырья. А именно:
- Спирт «Альфа» производят из пшеницы или ржи. Либо в данном случае применяют их смесь.
- Спирт «Люкс» и «Экстра» получают из разных видов зерновых культур, а также из их смеси или картофеля. Это зависит от индивидуального подбора сырья. Спирт «Экстра» получают исключительно из здорового зерна. Он предназначен для производства водки, которая идет на экспорт.
- Спирт 1-го сорта производят из смеси картофеля и зерна или просто по отдельности. Также в этом случае может быть использована сахарная свекла и меласса. Применение спиртов в промышленности способствует производству данного сорта спирта.
Расчеты указанного продукта осуществляются при помощи определения объема и температуры вещества в мернике. Специальным прибором (спиртометром) определяют плотность данного вещества. Она соответствует определенной крепости. При помощи специальных таблиц по полученным показаниям и температуре определяют крепость в % (оборот этилового спирта). Также здесь устанавливается соответствующий множитель. Он является немаловажным показателем. При умножении на него объема указанного вещества проводят вычисление количества безводного спирта, который в нем содержится.
В ГОСТе закреплены шесть основных физико-химических параметров безопасности. Установление предельных значений концентраций токсичных элементов изложено в СанПиНе. Наличие фурфурола не допускается вовсе. спирта неограничен. Однако при этом необходимо соблюдать все определенные условия.

Маркировка, упаковка и хранение
Указанный продукт разливается в специально оборудованные резервуары, канистры, бочки, бутылки или цистерны. Они должны герметично закрываться крышками или пробками. Тара опломбируется или опечатывается. Бутылки упаковываются в специализированные корзинки или ящики. Запрещено в данном случае использование стальной оцинкованной тары.
Этиловый спирт питьевой 95% разливается в стеклянные бутылки различного объема, которые герметично закрываются корковой или полиэтиленовой пробкой. Сверху надевается алюминиевый колпачок, на который наносится штамп предприятия-изготовителя. Также там указывается объемная доля спирта.
Непосредственно на бутылку наклеивается этикетка, на которой имеется название продукта, наименование и местонахождение производителя, торговая марка, страна происхождения товара, крепость, объем и дата розлива. Обязательно здесь же должна присутствовать информация о сертификации. Также на данную этикетку наносятся обозначения технической или нормативной документации, в соответствии с которой может быть идентифицирован продукт.
Затем бутылки укладывают в деревянные ящики. На них несмываемой краской в обязательном порядке должна быть нанесена следующая информация: название предприятия - изготовителя, наименование спирта, обозначение стандарта. Здесь же указывается масса брутто, количество бутылок и их вместимость. Также должны присутствовать надписи «Осторожно! Стекло!», «Огнеопасно», «Верх».

Этиловый спирт ректификованный, расфасованный в цистерны и резервуары, хранится вне производственных помещений предприятия. Данный продукт в бочках, канистрах и бутылях хранится в специализированном хранилище. Этиловый спирт представляет собой легковоспламеняющуюся летучую жидкость. Она по степени воздействия на человека относится к 4 классу. Поэтому к условиям его хранения предъявляются особые требования. В спиртохранилище бутыли и канистры должны быть размещены в один ряд, а вот бочки - не больше двух по высоте и ширине штабеля. Для того чтобы избежать взрыва, необходимо осуществлять защиту оборудования, резервуаров от статического электричества. Срок хранения в данном случае неограничен.
Итог
Ознакомившись с вышеуказанным, в полной мере можно узнать о том, как именно производится спирт этиловый, цена которого, в зависимости от вида продукции и литража тары, в которой он находится, составляет от 11 до 1500 руб.